耶鲁大学对涡虫的研究揭示,衰老并非仅源于细胞磨损,身体内部组织结构的“定位漂移”也是导致器官功能衰退的关键因素。
衰老是一个令全人类着迷且难以捉摸的过程。对于耶鲁大学文理研究生院的博士生 Andrew Verdesca 来说,研究衰老是一项既普遍又充满未知的挑战。在 Josien van Wolfswinkel 教授领导的分子、细胞与发育生物学实验室中,Verresca 与团队最近取得了一项令人意想不到的研究突破。
长期以来,人们普遍认为衰老主要是由于细胞层面的磨损和损伤。然而,这项针对涡虫的研究却提出了另一种解释:身体内部的“定位系统”一旦发生紊乱,导致细胞位置错乱,也会引发严重的生理退化。
研究对象是扁平虫,也就是俗称的涡虫。这种小生物拥有极其惊人的再生能力,即便被切成碎片,每一部分都能重新长成一个完整的个体。由于细胞能够不断更新,涡虫常被称为“近乎永生”的生物。但它们身上存在一个奇怪的矛盾:虽然寿命可以持续数年甚至数年之久,但它们的生育期却非常短暂,通常仅有短短几个月。
为了解开繁殖期缩短的谜团,研究人员通过显微镜追踪涡虫生殖器官随时间的退化情况,并尝试通过切割实验来观察其再生机制。令 Verresca 感到惊喜的是,如果将那些已经不再产卵、且至少一个月没有后代的衰老个体切成两半,让它们重新生长并成熟,这些新生的个体竟然能够再次开始产卵。
然而,即便如此,它们的生育窗口依然很窄。通过进一步观察,研究人员发现,涡虫之所以失去生育能力,并不是因为生殖细胞或器官本身磨损殆能,而是由于身体组织的组织结构出现了混乱。虽然每个分裂出的部分都能长出功能完备的新器官,但随着时间推移,这些器官的定位发生了偏移,例如卵巢会滑向错误的位置。关键细胞类型的丢失以及生殖组织间重要连接的断裂,导致整个系统最终走向瓦解。
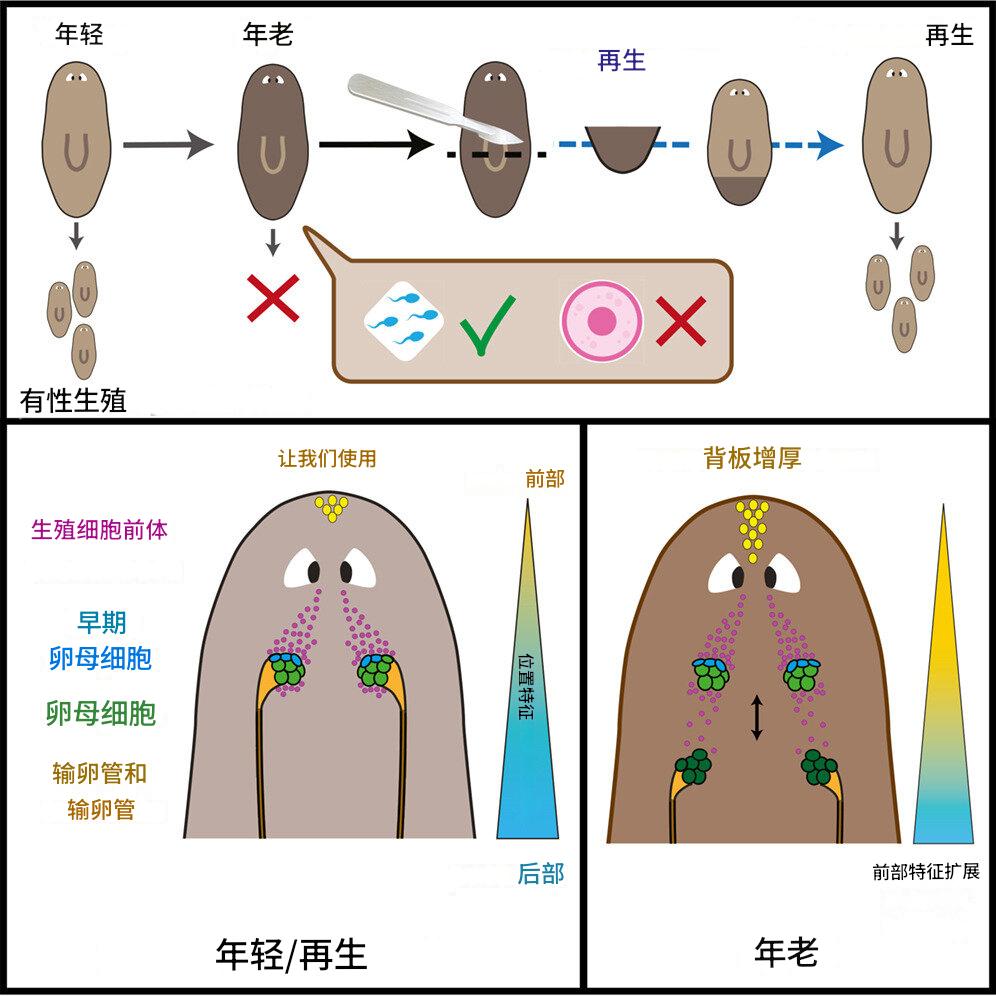
这一发现与此前关于“极性基因”的研究产生了共鸣。在包括人类在内的许多生物体中,这类基因负责指引器官应该生长在身体的哪个位置,实际上为身体各部位绘制了一张“位置身份”地图。虽然极性基因在胚胎发育中的作用已广为人知,但在衰老过程中的作用却鲜有研究。
研究人员通过实验进一步证实,由于极性基因及其发出的定位信号发生偏移,导致器官(尤其是卵巢)在错误的位置形成,从而引发了功能分裂和不育。通过人工改变极性基因的水平,研究人员成功地减缓或加速了涡虫生殖衰老的速度。
这项发现具有深远的意义。它表明,衰老的影响并不单纯是受损细胞的结果。即便像涡虫这样拥有强大细胞更新能力的生物,如果组织结构的组织架构崩溃,其功能依然会衰退。如果能够重新校准这种组织结构,或许能为管理人类的衰老过程提供全新的思路。
耶鲁大学分子、细胞与发育生物学副教授 van Wolfswinkel 表示,涡虫可以利用再生能力来重置空间信息。未来的研究将致力于探索导致“位置漂移”的具体原因,这可能为人类等其他生物维持年轻状态提供新的策略。